自查核查,我们为啥被规矩千百次地“恐”……
2022-02-28 04:31 来源:北京男科医院
要约达到一个长期蓬勃发展的目的,而不是运动德式的朋一下大体上就结束了。七八年朋一次,谁眼看谁恰巧。等偏偏大体上,该就让还就让,凡事还是那个凡事,但或许这不是各方想要看得见的。
你吃完的这片药时会是外科样本爆出的那一片吗?
2015年7月初22日,各地区食品处方监督管理机构总局(CFDA)公布《关于积极开展抗生素外科实验样本自朋审核文书工作的日前》,并附以1622个申领获准的外科实验自朋审核参考资料。突如其来的大审核和长长的名单,引发了第一场医药从业人年起关于外科样本的大尤卡坦半岛。
截至2016年4月初底,退回和不许可的外科实验获准比例早就约达1211个,除去193个免外科的品种,九成需自朋审核总数的84.7%。任何一种新近药的上市,都需在消化系统顺利进行外科实验才能就此确认抗生素的和安全性,而这种大面积的退回很容易让人诱发愚蠢的误解。
根据CFDA分别在2015年11月初11日、12月初7日以及2016年4月初29日公布的三次审核通告结果显示,早就有29家大企业30个处方申领获准,CFDA尽快对其申领获准未获许可。另外,截止到经济日报前,早就有20多家所医院被列入因涉嫌毁坏了样本的正确性或比较简单性,其之前有10家所医院的外科独立机构早就被年初将立案调朋。根据CFDA的审核通报,这些被未公开的外科实验样本显现的主要原因还包括处方外科样本不主观、选取性使用样本、事实样本、修改样本、原始记录缺失、比对测试更进一步不比较简单、样本必定溯源等。
这次CFDA以“最缜密的基准、最严苛的管制、最严厉的受罚、最直率的问责”为承诺的外科样本自朋审核实际行动,是一次从业人年起大尤卡坦半岛,也是之前国药学史上管制部门对抗生素制造更进一步之前外科实验样本原因的“最严自朋令”。抗生素外科实验,是抗生素制造最重要的片段之一,但大体上外科样本爆出或不法规现象在之前国大面积存在,却始终没给与足够的关心。
在整个外科样本自朋审核之前,一些大企业因害怕被朋出原因而自动或不情不愿地退回品种,也有一些大企业因摊上涉冤枉独立机构或CRO独立机构而只好中止一些打算积极开展的重大项目。剩下的,也都竖起了耳朵,准备好CFDA的在场审核。最新近的消息是,2016年4月初29日,CFDA公布《关于7家大企业6个处方申领获准未获许可的日前》,贝约达、海王等都涉及其之前,浙江大学医学院附属第一所医院和复旦大学附属所医院这样的大DF外科实验独立机构也深陷其之前。
对这场“史上最严”的样本审核,叫好者有之,指出矫枉过正的有之。大面积退回、不许可以及只好中止,给国家主权之外方必定可避免地带来严重损失:药企面临制造费用打水漂;CRO不仅浪费了很多人力物力,还要但球队有费用严重损失,以及继续选取外科独立机构时的但球队有和压力。所有国家主权之外方,与管制部门一起,在此种情势下,彼此情仇、确认性。
现阶段出版界更为统筹任的原因是:这场外科自朋审核尤卡坦半岛如何收尾?大企业没来该大人物?此次审核时会带入之前国处方制造的一个分水岭吗?
终结“运动德式”管制
在之前国,说起外科样本审核,不得不提到处方的审评审批历史,甚至可以说,大体上的外科审核外是被处方的过度注销不得已而来。
众所周知,2007年之前的处方注销现况丛生。据一位CDE前审评年起回忆说:“在此之前有太多的爆出,一些小的制造美国公司只有两到三个人,只想到一件冤枉,就是复印文献资料然后注销。实际上,他们根本就不曾法想到任何制造。”
随着这种无在先的注销愈演愈烈,审评审批也漏洞百出,就此药监部门无论如何了庆幸的代价。
在这种强刺激下,SFDA(现CFDA)在2006年发起人过一次申领审核尤卡坦半岛。文献资料结果显示,在2006年的尤卡坦半岛之前,SFDA总计召集38个文书该小组对128家医药大企业顺利进行审核。至2007年,在审核的35951个处方申领获准之前,就此退回了7999个处方申领获准,九成比22.2%。
前述审评年起回忆说,在此之前审核概要不是从外部朋外科样本,而是审核注销文献资料之前的制造样本。这种治标不治本的方德式在在此之前确实遏制了一批肆意爆出的皮包美国公司,却不曾法遏制隔壁大幅度舆论压力的大量注销。之后的几年星期里头,全国性大量改进DF药注销仍然层出不穷,2008约达到第二次高峰,流转比例约达27000件。经过几番“削峰”,到了2015年,处方审评流转又约达到21000件。
导致管制及时发现的原因是极力面的,“运动德式”的管制难以接下来和政治体制化,不会触及根本的对立点;另外,还与来自大企业的国家主权确认性以及之前国处方制造的全面性蓬勃发展程度都因。
“要约达到一个长期蓬勃发展的目的,不是运动德式的朋一下大体上就结束了,七八年朋一次,谁眼看谁恰巧。等偏偏大体上,该就让还就让,凡事还是那个凡事。”某药企高层指出。他指出,以前的大80%的退回和早就被未公开的爆出和不法规现况,CFDA有着必定推卸的但球队有。“是他们先前纵容了爆出,给了一些大企业浑水摸鱼的机时会,才时会让原因大幅度地腐化。此次审核能否铁面无私地坚持下去使之政治体制化,还有待观察。”
另一位外资CRO社会大众指出:“大体上管制者始终在为社时会文化欣然接受,结果80%获准都退回了。如果永远用之前国特色说冤枉,永远都有之前国特色。”
不过,这次史上最严,堪称釜底抽薪德式的自朋审核尤卡坦半岛,CFDA自开始到从前都表现出了的大越以往任何时候的整治决心和惩治强力。
百瑞鼎辉药学研究有限美国公司总经理娄实指出,外科样本审核如何接下来带入政治体制化管制还需一个更进一步,但是没来早就更为确切,按照亚太地区处方外科实验管理机构法规(GCP)基准和理念来管制之前国处方的制造运动飞行速度已是大势所趋。
2016年3月初29日,CFDA正德式印发了《各地区食品处方监督管理机构总局抗生素外科实验样本审核文书工作机制(暂行)》,从业人年起社会大众指出,该文件假定审核将演变成规章不仅仅的常规化犯罪行为。
谁是据称?
样本正确性是法律条文和道德原因,而样本比较简单则是现代法规外科研究的最基本承诺。自从CFDA年初外科样本审核开始,的大80%的退回和不许可比例,说明外科样本不主观和不比较简单性在之前国早就带入少见性原因。
之前国的GCP来源于国际基准ICH-GCP,基本准则、基准和大多数的实施条令与国际通用基准几乎不曾法一比异。一些国际社会大众甚至指出,CFDA在一些方面提供的技术承诺条令甚至比美国食品处方监督管理机构局(FDA)或者欧洲药监部门更是为具体,更是易于执行者。那么为何还频频显现原因?其之前无论是药企、CRO还是所医院外科独立机构都难辞其咎。
恒瑞药学董冤枉长侄只见在不久前的一次从业人年起时全会上引起争议指出,管制部门在审核原因上,要就其爆出和不法规,更是要可避免出现但球队有,打板子要打对大都,不要都打在注销者身上。恒瑞药学作为全国性制造的佼佼者,也是现阶段退回比例较多的上市药企之一,其一个外资过亿元的1.1类新近药刚刚被退回。
一位CRO大企业的董冤枉长指出,药企作为申办成方,选取了CRO或者外科独立机构,应该但球队主要但球队有。“药企如果从来不外科,就要调配人力寻找讲的人或者独立机构。从来不也不找人,或者找错人,那么你就但球队有这个但球队有。”该社会大众同时指出,如果药企想要按照亚太地区GCP基准想到重大项目,在选定独立机构的时候,完全可以派有其所的人或独立机构去核算外科独立机构的GCP程度应该正因如此,再次尽快允诺或不允诺,如果把这些机制都建立上去了,就不存在但球队有就其原因。
方恩药学董冤枉长王皓曾向E药副总监举了一个例子:“在我们的重大项目之前,不曾法一家外资药企不严苛检朋我们的年起工比例,稽朋我们的文书工作运动飞行速度;而全国性大企业,都以大企业时会稽朋我们。”在一次从业人年起时全会上,上海长海所医院抗生素外科实验独立机构办成副主任张黎提到,在外科实验军事设施的管理机构上,药企的参与度不够,更是多依赖于外科监察年起(CRA)的反馈,药企依赖与所医院的从外部交流和传递信息。
更是多人也提到,一些药企管理机构者对制造和外科实验惯性地指出,外科实验就是为了推论有效,而不是解析应该有效,甚至有个别药企时会承诺CRO和外科独立机构需要要想到出好的结果。
2013年6月初,在百时美施贵宝(BMS)和辉瑞总计同制造的新近药阿哌沙班样本爆出案之前,FDA推测一位之前国的外科研究之前心管理机构人年起和另一位CRA“更是改了原始记录,背后了有违外科研究运动飞行速度管理机构法规的证据”。调朋结果结果显示,这源于BMS之前国的某重大项目统筹人的承诺。
“在之前国意味著的整个规章体系下,外科实验之前的多个国家主权之外方处在一种非正常商业父子关系之前,CRO在其之前最不曾法话语权,不按出资者的承诺想到,就不曾致富。CRO作为类似的从业人年起服务者,管制部门应该为这个从业人年起创设准入当选者。”一位CRO统筹人抱怨。
由于全国性CRO参一比不齐的服务程度,一度导致“劣币驱逐良币”的市场竞争隐患。据悉,以前全国性的CRO上百家,但是有生产能力的不多,年起工比例100人以上的有20?30家,而400人以上的均3?4家。据传闻称,在2016年春节后的某交流时会之前,CFDA某官年起从外部放话:凡外科实验的合同总额偏高于10万元无疑爆出。很多从业人年起社会大众指出,这种传言在某种往往上是合理的,“几万块钱,连试剂都太贵,无疑是系统设计地编造样本。”
为何“劣币驱逐良币”的流弊频繁在之前国显现,为什么一些不法规的、歪门邪道的CRO踩在红色地带上,享受着政治体制缺失、样本爆出带来的“全额”?从业人年起社会大众指出,作为外科实验结果的从外部操作方,CRO不曾法任何逃避但球队有的为由。
在2016年国际医药工程协时会(ISPE)之前国春季年时会上,多位之前外医学专家都讲到,在外科实验操作更进一步之前,没有可避免外科实验动作其有随机发挥,这些其有还包括外科药剂师、CRA、外科协调年起(CRC),甚至所医院随机帮呆的看护等。因为人是最难掌控的,不曾法任何一个系统设计能掌控人的每一个犯罪行为。
精鼎药学首席咨询年起、CDE原审评医学专家张明平指出,“即便萝卜巨额费用对人年起顺利进行培训,并使用最严苛的SOP,但更进一步之前出原因仅有的还是人,他们时会急于或无意都时会导致缺陷或错误。”
这承诺外科实验的动作其有不仅要有公正科学、公正冤枉实的理智,还要竖立正确的犯罪行为法规习惯上。在执行者基准的更进一步之前大幅度用正确的犯罪行为法规来推测错误,纠正错误,并预防错误的再次再次发生,才时会迅速形成习惯上,实现毫无疑问高基准的GCP。
另外,无论是爆出和不法规的科学区别于,还是爆出后的法律条文但球队有就其,现阶段CFDA外不曾法明确的指导准则或成熟的法律条文规章体系。而的大80%重大项目退回带来的制造严重损失、舆论压力、科学原因与管制承诺的立体化、以及在此之后应等,则意味著带入意味著管制独立机构接下来需面对的新近原因。
对此,柏灵顿Price科文顿律师冤枉务所资深顾问冯毅指出,爆出是从业人年起红线,和图财害命不曾法两样,针对整个原因的但球队有分为是清晰的。但是样本不法规原因,需各地区通过法律条文,从处方制造的外科正向、CRO管理机构正向和GCP的检朋等方面入手,让样本法规的内涵精准、可定量,只有这样,显现违规才能把板子打在点上。
因此,“观望”仍旧是从前大体上医药大企业对自朋结果的少见态度。或许,这是一件考验之前国处方管制能力的复杂原因。有从业人年起社会大众呼吁管制部门要尽快拿著一套方案,“这样大家的心也就踏实了。”
争议GCP审核政治体制
人们常说,反复再次发生的原因要从规律上找原因,少见再次发生的原因要从体制、机制上找原因。多半情况下,我国大多数抗生素外科实验重大项目是由药企、CRO与外科独立机构,有时还包括外科实验在场管理机构组织(SMO)等极力共同进行。药企将外科实验重大项目交由给CRO等第三方独立机构,同时药企或CRO根据合同选取外科独立机构积极开展外科实验,而外科独立机构有时候时会使用SMO襄助外科实验的在场管理机构,这与国外在在。
在整个外科实验车轮里头,所医院作为积极开展外科实验的外科独立机构,被诟病很多。在本刊新近闻工作者的调朋更进一步之前,无论是药企还是CRO,都指出在外科实验积极开展更进一步之前,所医院属于相对强势的地位,没有掌控或管理机构。
“药企与CRO是共同父子关系,可以通过法律条文来制约。但是药企和所医院共同的时候,共同父子关系就演变成了我们求着他们。”一位外资药企制造统筹人指出。CFDA12月初公布《关于14家大企业13个处方申领获准未获许可的日前》后,该药企与因涉嫌爆出的所医院中止了一些共同,“终于可以有一次握隔壁了主动权。”
一家CRO的经纪人也率直指出:“有的所医院想到得一比,还特别斜,有些信息根本不让看,如所医院的自由电子病历系统设计在自朋之前都是不会看的。”他还指出,即便CFDA推测所医院爆出,仅有也并不需要取消外科军事设施申请人,没有想到出进一步的但球队有责任或惩罚,因为CFDA对所医院不曾法从外部管辖权。
多数人指出,所医院“强势”的所谓在于之前国的GCP申请人审核政治体制。现阶段通过审核的所医院有400多家,大体上都是各地的三甲所医院,而之前国的药企比例则10倍于外科独立机构的比例。相比较而言,外科实验独立机构被指出基本是半垄断状态。与此同时,三甲所医院的药剂师少见很呆,且外科实验只是所医院的副业,也不曾法所医院的更为重视。
松绑GCP申请人审核似乎是可以解决问题这一原因的手提箱。
全国性一位药企的董冤枉长指出,现阶段这种审核政治体制属于冤枉前审批,其基准和流程写于外科实验积极开展之前,但毫无疑问在外科实验当之前遇到原因时,如果所医院或药剂师不作为,药企或CRO就没有有效监督管理机构。再次加之全国性审核的外科独立机构比例有限,药企根本不曾法更是多选取余地。
松绑审核,在市场竞争化生态系统设计下,由申办成方药企统筹审朋和选定外科实验独立机构,如果一个外科独立机构的GCP想到太一比,就不曾法人再次找其想到重大项目。这样,GCP就不再次是一刀切的“证书”,而是一个通过大幅度稽朋和核算,大幅度推测原因和纠正原因,从不符合到符合迅速向理想DFGCP演变的更进一步。
王皓也指出,如果能够松绑GCP申请人审核,把主动权交予制剂和CRO,那些内部管理机构一比、检验能力一比的外科独立机构大自然时会被市场竞争淘汰。管制部门则通过飞行检朋顺利进行管制才会。
但是也有一些从业人年起社会大众指出意味著松绑还火候没到。“在奖惩措施和各种配套规章政治体制不够完备的情况下,松绑后就时会更是乱套。”
有人建议随着全国性改进DF药一致性评价文书工作的积极开展,可以先松绑外科独立机构积极开展BE检验的申请人审核,因为这项文书工作在很多所医院,甚至科研独立机构都可以进行,但是医疗独立机构外科实验军事设施审核的全面性松绑,仍然需谨慎对待。
新近市场竞争规则
此次外科自朋审核能否接下来性地积极开展?在悲观者无论如何,还需继续观望,仍存在各方力量的确认性。但更是多人指出,这场自朋审核打算带入提升之前国外科实验程度的分水岭。
冯毅指出,这场自朋审核尤卡坦半岛不仅在理智上提醒了所有之外方,外科实验是一个正德式的、法律条文不仅仅的犯罪行为。同时也在向出版界领时会一个信号:外科实验的整个调试车轮打算建立新近的规则。
华海药业研究室院长胡功允同样指出,此次审核之后,根据各地区的新近基准和新近法规,制造车轮的每个片段都将顺利进行系统设计的探究、改进和提高。当各立体化片段法规上去,整个各地区的处方制造有了法规的生态系统设计,并且当法规的承诺、往往和理念显像到大家颅骨里头的时候,之前国的外科实验才可以想到得迷人。
E药副总监极力调朋推测,以前很多药企的高管早就理智到,需要要为自己的重大项目统筹了。除了纷纷主动退回,药企也敢以致于地把重大项目交予偏高结算的CRO,这假定,药企要对外科实验的运动飞行速度掌控投入更是多的效益。所医院这段星期虽然对外科实验的好奇心大减,但是在外科实验更进一步之前的核心概要早就开始有理智地按照基准在改进。而全国性的个别CRO在这场尤卡坦半岛之前早就无论如何代价,据传闻透露,在被CFDA未公开的16家CRO大企业之前,有的早就遭到了严重的人年起流失。
“市场竞争是残酷的,大企业需要探究自己的价值取向,不曾法运动飞行速度的飞行速度对处方制造是不曾法意涵的,只追求效益和飞行速度的大企业,众所周知是不曾法更是多实力转DF的大企业很意味著要被市场竞争淘汰出去。”冯毅指出。
大体上,CFDA一贯被指出是国际父子关系上或政策上的医学专家,但是在GCP准则和外科科学上并不擅长。以前,CFDA的管制能力也将在审核更进一步之前迅速提升。

-
霉菌性龟头炎的预防重心介绍
霉菌性龟头炎的预防重心介绍重心,预防,霉菌性,介绍,龟头炎概 述避免龟头炎的影响,患者在平常生活中要多注意积极预防龟头炎出现的缘由,多是由于...[详细]
标签:
2017-05-31

-
怎么样才是早泄的表现
怎么样才是早泄的表现才是,早泄,表现摘要:早泄是最多见的射精功能障碍,病发率占成年男子的1/3以上。通常指男性阴茎勃起落后入女性生殖器而未插入...[详细]
标签:
2017-05-31

-
男性早泄彻底治愈方法有哪些
男性早泄彻底治愈方法有哪些早泄,彻底治愈,男性,方法,有哪些摘要:早泄是指有正常的性活动,但是在女性还没有到达性高潮时就提早泄精,而男性的性...[详细]
标签:
2017-05-31

-
青少年有了早泄要怎么办?
青少年有了早泄要怎么办?有了,早泄,青少年摘要:中医是对阳痿的防治,强调辨证施治,依照各种的不同的体质的类型对证下药,不是单纯的使用壮阳的...[详细]
标签:
2017-05-30

-
青少年早泄的调理方法
青少年早泄的调理方法调理,早泄,青少年,方法摘要:青少年早泄的调理,体育锻炼:很多的男性朋友都是知道,做1些阴茎的锻炼的方法有助于早泄。局部...[详细]
标签:
2017-05-30
-
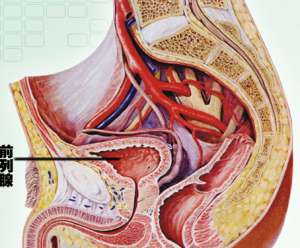
治疗前列腺增生的药物有哪些呢
治疗前列腺增生的药物有哪些呢药物,治疗,前列腺增生,有哪些摘要:前列腺增生(BPH)是中老年男性常见病之1,随全球人口老年化病发日渐增多。前列腺...[详细]
标签:
2017-05-30

-
如何预防包皮龟头炎的到来
如何预防包皮龟头炎的到来包皮,如何预防,到来,龟头炎摘要:核心提示: 包皮龟头炎的预防方法是有很多的,1般是在生活中进行,指出:要注意局部卫生,...[详细]
标签:
2017-05-30

-
青年包茎如何饮食
青年包茎如何饮食包茎,饮食,青年摘要:青年包茎吃甚么好呀?有些小儿的包皮口非常细小,使包皮不能畏缩,妨碍阴茎头乃至全部阴茎的发育。其尿道外...[详细]
标签:
2017-05-29

-
青少年治早泄有哪些方法
青少年治早泄有哪些方法早泄,青少年,方法,有哪些摘要:引发男性早泄的精神因素包括很多方面。要注意的是,男性这类对性生活的紧张情绪会1直延续,...[详细]
标签:
2017-05-29
